Стернальная пункция и исследование миелограммы при лейкозах
Казалось бы, о состоянии системы крови можно и нужно судить по общему анализу – с детства известной рутинной медицинской процедуре. Но на самом деле, данные этого анализа — отражение процессов, происходящих в кроветворной системе, и ее главном органе – костном мозге. Поэтому при подозрении на болезнь кроветворной системы анализируют состояние костного мозга. Пункция костного мозга – это вмешательство, которое позволяет получить 0,5-1мл. этой субстанции для дальнейшего исследования.
Что такое костный мозг и зачем его изучают?
Красный костный мозг находится в плоских костях – ребрах, грудине, позвонках, костях черепа и таза – и в эпифизах (концевых частях) трубчатых костей. Он состоит из двух типов клеток – стромы, или, говоря простым языком, основной структуры, и кроветворных ростков из которых, собственно, и формируются форменные элементы: эритроциты, лейкоциты и тромбоциты.

Все элементы крови развиваются из одинаковых стволовых клеток-предшественников. Созревая (в медицине этот процесс называется дифференцировкой), клетки формируют два ростка кроветворения: лимфоидный, из которого потом созревают лимфоциты и миелоидный, создающий остальные форменные элементы. Незрелые клетки крови называются бластами. Обычно 90% всех стволовых клеток находятся в состоянии покоя.
В организме взрослого мужчины в сутки созревает 300г. форменных элементов крови, то есть 9 кг за год и около 7 тонн за 70 лет жизни. Новые клетки формируются взамен состарившихся или погибших по другим причинам (например, в борьбе с инфекциями).
В норме количество вновь созревших клеток строго равно числу погибших. При гемобластозах (лейкозах) клетки кроветворного ростка мутируют, перестают реагировать на регуляторные сигналы организма, и начинают бесконтрольно делиться. Если активность этого процесса настолько велика, что вновь сформированные клетки не успевают созреть, лейкоз называется острым. Если преобладают зрелые формы – хроническим.
Прежде чем выйти в кровоток, измененные лейкозные клетки накапливаются в красном костном мозге. И только инфильтрировав (заполонив) его, поступают сосуды. Изменения в анализе крови далеко не всегда соответствуют происходящему в костном мозге: на некоторых стадиях развития лейкоза количество форменных элементов в крови может не только не увеличиваться, но и уменьшаться.
Если же баланс нарушается в другую сторону, и созревание клеток крови не успевает за их гибелью, формируются анемии, тромбоцитопении, лейкопении. И опять изменения в периферической крови могут «не поспевать» за процессами, происходящими в костном мозге.
Именно по этим причинам пункцию костного мозга и миелограммы выполняют при подозрении на любые болезни кроветворной системы.
Как и для чего выполняют пункцию костного мозга?
Чтобы получить материал для исследования, нужно проткнуть (пунктировать) кость там, где она находится близко к коже. В зависимости от возраста (а количество костного мозга в разных анатомических структурах изменяется со временем), это могут быть:
- у детей младше 2 лет – пяточная или большеберцовая кость;
- у детей старшего возраста – гребень подвздошной кости;
- у взрослых – грудина или гребень подвздошной кости.
Игла для стернальной пункции
Прокол делают специальной иглой с ограничителем – иглой Кассирского.
Она может выглядеть по-разному. Но суть в том, что ограничитель позволяет зафиксировать глубину прокола.
Методика
Пункцию ребенку обычно делают под общей анестезией, «наркозом». Взрослому – под местной. Обезболивающим «обкалывают» не только кожу, но и надкостницу, тем не менее момент непосредственной аспирации (всасывания) пунктата, довольно болезненный. Из полученного пунктата делают мазки для исследования под микроскопом и пробы для автоматического подсчета клеток.
Иногда полученный материал бывает неинформативен. Тогда (и при некоторых других показаниях) делается трепанобиопсия – метод, при котором специальной толстой иглой одним блоком забирают не только красный костный мозг, но и участок костного фрагмента над ним. Такую биопсию обычно делают в области гребня подвздошной кости.
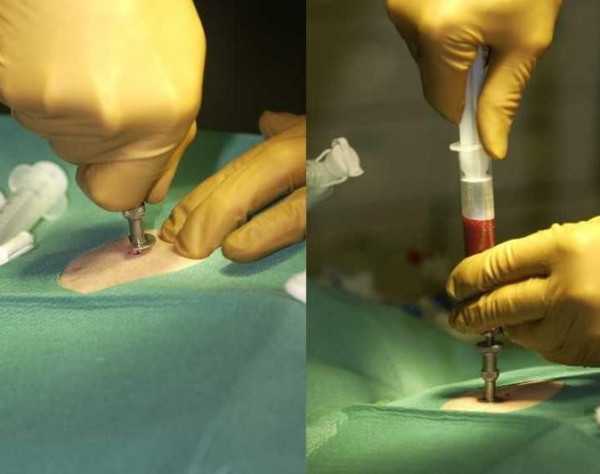
Место прокола закрывается стерильной повязкой или пластырем. Боль может беспокоить и некоторое время после процедуры. Если нет противопоказаний, можно принять обезболивающие. Место прокола нельзя мочить в течение суток, соответственно, не рекомендуют принимать душ или ванну. Какого-то дополнительного ухода после пункции костного мозга не требуется.
Противопоказания
Процедура эта безопасна, единственное абсолютное противопоказание – тяжелые нарушения свертывающей системы крови, когда любая травма приводит к обширным гематомам. Относительные противопоказания (когда сравнивают возможную пользу и вред), это:
- острый инфаркт миокарда;
- декомпенсированная сердечнососудистая патология;
- гнойные поражения кожи в области предполагаемой пункции.
Возможные осложнения
- кровотечение;
- инфицирование;
- аллергия – при непереносимости обезболивающих средств;
- сквозной прокол грудины, перелом (если пункция выполняется из грудины).
Вероятность осложнений невелика – по данным Британского общества гематологов за время с 1995 по 2001 год на 54890 проведенных пункций пришлось 26 осложнений разной степени тяжести.
Расшифровка и оценка результатов: миелограмма.
В первую очередь, в счетной камере подсчитываются мегакариоциты и миелокариоциты.
Миелокариоцитами называют те клетки костного мозга, содержащие ядро, то есть подсчет их – это оценка «клеточности» костного мозга, активности кроветворения. В норме — 8тыс. – 150тыс. в 1 мкл.
Мегакариоциты – это крупные клетки с большими ядрами, предшественники тромбоцитов. Их должно быть более 20, но менее 50 в 1 мкл.
Далее в окрашенных мазках подсчитывают процентные соотношения клеток различных рядов кроветворения. Полученный результат называется миелограммой.
Непосредственно перед подсчетом мазок обязательно рассматривают при небольшом увеличении – это позволяет оценить картину «в целом», увидеть патологические опухолевые клетки.
Итак, отвечая на вопрос «нормальная миелограмма – что это такое», нужно сказать, что это процентное соотношение кроветворных клеток на разной стадии созревания.

Чтобы оценить по миелограмме качество костного мозга, важно знать не только процентное и количественное содержание гемопоэтических (кроветворных) элементов, но и их соотношение. Вот расшифровка некоторых показателей.
Индекс содержания лейко/эритро или соотношение между предшественниками белых и красных кровяных клеток.
В норме 2:1 – 4:1. Если индекс увеличен при «богатом» костном мозге, это, скорее всего, говорит о чрезмерной активности белого ростка (например, развернутой стадии хронического лейкоза). Увеличение индекса при «бедном» костном мозге может стать показателем сниженной активности красного ростка (апластических анемиях). Если индекс снижен при «бедном» костном мозге, это может быть показателем чрезмерной активности красного ростка кроветворения или о снижении активности белого ростка.
Индекс созревания нейтрофилов.
Высчитывается по формуле: (Промиелоциты + миелоциты + метамиелоциты) / (Палочкоядерные + сегментоядерные нейтрофилы). Нормальное значение 0,6 – 0,8.
Повышение индекса при «богатом» костном мозге свидетельствует о задержке созревания нейтрофилов (к примеру, при хроническом миелолейкозе), при «бедном» костном мозге – о чрезмерно активной продукции (и расходе) зрелых клеток и истощении резерва кроветворение – подобная ситуация возможна при тяжелом сепсисе. Снижение индекса при «богатом» костном мозге может означать ускоренное созревание гранулоцитов или их задержку в костном мозге.
Индекс созревания нормобластов.
Формула расчета: (Полихроматофильные + оксифильные нормобласты) / (Все ядросодержащие клетки красного ростка этого пунктата). Норма 0.8 – 0.9 и снижение индекса говорит о чрезмерно медленном наполнении гемоглобином эритроцитов (например, при железодефицитной анемии).
Как и у любого инструментального исследования, референсные значения (нормы) миелограммы могут изменяться в зависимости от лаборатории и используемых аппаратов.
Особенности миелограммы при лейкозах.
Лейкемический клон, активно делясь, нарушает нормальный гемопоэз (выработку и созревание клеток крови). Патологические клетки вырабатывают вещества, подавляющие размножение и дифференцировку других ростков кроветворения. Отягащяющим фактором является то, что эти клетки «захватывают» все ресурсы, и на нормальные форменные элементы резервов организма просто не хватает. Поэтому при любом лейкозе в костном мозге преобладают опухолевые клетки, какие именно – зависит от вида лейкоза, а клетки других ростков кроветворения будут присутствовать в количествах значительно меньших, чем нормальные. При остром лейкозе главный диагностический критерий – 25% и более бластных клеток. При хроническом лейкозе число бластов остается в пределах нормы или незначительно повышено, резко увеличено количество клеток пораженного ростка на разных стадиях созревания. Например, при хроническом лимфолейкозе увеличивается количество лимфоцитов, при миелолейкозе – промиелоцитов, миелоцитов и миелокариоцитов и так далее.
Как при остром, так и при хроническом лейкозе усиленный рост патологических клеток сопровождается уменьшением количества эритроцитов и тромбоцитов на всех стадиях созревания.
Если в миелограмме видны признаки лейкоза, пунктат костного мозга дополнительно проходит иммуногистохимическое, цитохимическое и генотипическое исследования – они нужны чтобы определить характерные особенности мутации опухолевого клона. Это важно для выбора схемы лечения конкретного пациента.
rosonco.ru
что это такое, норма, обозначение, определение, инвитро
Для того, чтобы вовремя определить есть ли у пациента онкологического заболевание обычно делается анализ крови на рак, лейкоз. Если врач обнаруживает бластные клетки в анализе крови, то это считается признаком наличия у пациента острого лейкоза в крови.
Что это такое
Бластные клетки в анализе крови, что это такое? Они представляют собой незрелые клетки, из которых затем образуются нормальные кровяные тельца. В норме в кровеносной системе они не встречаются, а находятся всегда в костном мозге, поэтому после проведения этого анализа проверяют и костный мозг на наличие нормобластов.
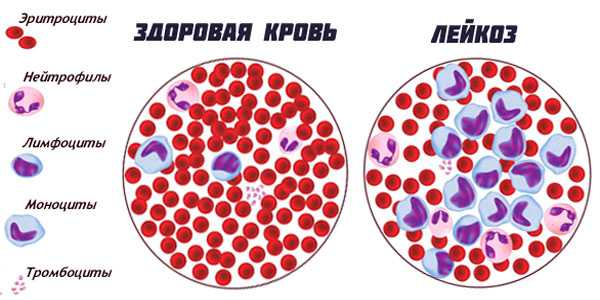 Нормальная кровь и при лейкозе
Нормальная кровь и при лейкозеРазновидности лейкоза
Медицина подразделяет лейкоз крови на две разновидности – это хроническая форма лейкоза (состоит из зрелых и незрелых элементов), причём никогда не переходит в острою форму лейкоза (при ней обнаруживаются бласты в составе крови). Эти клетки при остром лейкозе являются опухолевой составляющей в организме человека.
Обычно такая форма заболевания имеет название от клеток, предшественниками которых являются незрелые бластные клетки, например, это могут быть миелобласты, лимфобласты, монобласты, эритробласты. Таким образом, выделяют острый миелобластный лейкоз, острый лимфобластный лейкоз и другие формы рака крови.
Врачи во всём мире используют определение и обозначение бластных клеток в анализе крови с помощью международной системы ФАБ, которая предусматривает характеристику острого лейкоза по степени полиморфизма, по форме ядра бластов, в зависимости от созревания бластов или без их созревания.
Определённых симптомов бластных клеток в организме, по которым можно определить наличие лейкемии в крови, не существует, но чем раньше вы почувствуете недомогание, сдадите общий анализ крови, тем быстрее специалист сможет выявить данную патологию. Следует помнить, что острая форма лейкоза крови, в большинстве случаев встречается у детей.
Особенности анализа
Для диагностики острой формы лейкоза, необходимо сдать общий анализ крови и по нему специалист определит какие заболевания есть у вас в наличии. Если количество эритроцитов понижено, то говорится о нормохромном характере анемии. Скорее всего, при таком анализе на бластные клетки будет выявлено и пониженное количество тромбоцитов. В редких случаях их количество сильно увеличено, и они имеют ядра причудливой формы. СОЭ (скорость оседания эритроцитов) при острой форме лейкоза повышена, но бывают случаи, когда она находится в норме.
 Система автоматического анализа лейкоцитов
Система автоматического анализа лейкоцитовСледует знать, что в норме бластные клетки в анализе крови отсутствуют, так как они находятся в костном мозге и не выходят за его пределы. Первым симптомом лейкоза крови, однако, является высокий уровень лейкоцитов, которые находятся в крови вместе с бластными клетками.
В любом случае, по одному общему анализу крови, диагноз лейкемия не ставится. Если цитопения непонятна, то в обязательном порядке берётся из костного мозга исследование в виде пункции.
Бывают случаи, при которых данная процедура, что тромбоциты в норме и бластные клетки в крови отсутствуют, и при взятии из костного мозга пункции определяется, что бласты тоже в пределах нормы, но, если специалист имеет сомнения в диагнозе, то делается трепанобиопсия, которая находит в крови пролифераты клеток, по ним и определяется наличие или отсутствие заболевания.
В инвитро, бластные клетки в анализе крови определяются разными способами и проводятся повторное тестирование крови, которое поможет поставить правильный диагноз.
Проведение анализа
Анализ на бластные клетки, на рак, как всегда, сдается утром натощак и специальной подготовки к нему не требуется. Проводят забор крови из вены.
Если анализ крови на лейкемию берется с утра, то в лаборатории намного легче определяются нормобласты и другие клетки, указывающие аномальные отклонения в организме больного. Конечно, такое исследование проводится по желанию пациента, если он начал замечать у себя плохое самочувствие и другие признаки болезни. Однако следует помнить, что острая форма лейкоза у женщины и мужчины проходит обычно стремительно, поэтому, чем раньше была проведена диагностика, тем лучше.
Эта болезнь, в большинстве случаев, встречается у детей, поэтому выявить аномальные клетки, которые быстро распространяются в организме можно легко. Поэтому врачи советуют родителям регулярно сдавать детям такой анализ на исследование крови направлению педиатра.
sostavkrovi.ru
Нормы бластных клеток в анализе крови, диагностика и расшифровка результатов
Анализ крови – главное и первое исследование, которое назначают врачи при поступлении пациента в больницу. Он полно, быстро и дешево выдает объем информации о состоянии больного. Однако такие анализы различны, один из вариантов – исследование на количество бластных телец. Что это, зачем они нужны и какой нормальный уровень в крови? Разберемся!
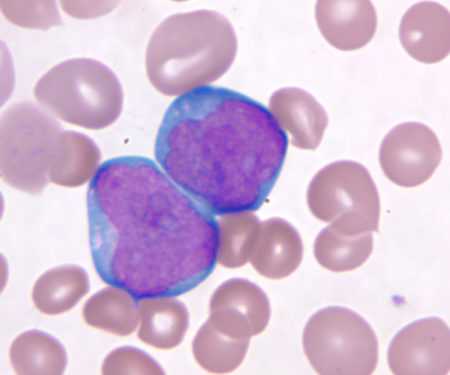 Определение клеток под микроскопом
Определение клеток под микроскопомЧто такое бластные клетки?
Кровь – важнейшая жидкость в организме человека. Выполняет множество функций,: от питания до защиты органов от инфекций и бактерий. За каждую «задачу» отвечают клетки крови, например: эритроциты – красные кровяные тельца, доставляют кислород в уголки человеческого тела.
Предшественниками элементов крови являются бласты. Развиваются в спинном мозге и по мере необходимости превращаются в эритроциты, лейкоциты и так далее. Здоровые тельца готовы «преобразиться» во время острых кризисов в больших количествах, появляясь в крови в виде защитных или других клеток.
Что такое острый лейкоз?
Острый лейкоз – следствие нарушения в работе кроветворения на сначальных стадиях. В нормальном состоянии бластные клетки превращаются в функциональные клетки крови и выполняют свою миссию. Каждое такое тельце сразу после «появления на свет» имеет свою линию развития. Например: для эритроцитов «производятся» один вид таких клеток, а для лейкоцитов – другой и так далее.
Когда кроветворная система дает сбой, и создание здоровых базовых клеток нарушается, тельца ведут себя по-другому. Они не превращаются в «рабочие» клетки – только потребляют полезные вещества и размножаются. Со временем заменяют здоровые клетки и проникают в кости, разрушая их, не поставляя полезных веществ. Резко снижается количество полезных клеток, падает гемоглобин, тромбоциты и лейкоциты.
Такая болезнь лимфобластная и миелобластная – в зависимости от того, какой тип клеток стал «виновником» заболевания. Подразделяются на другие, более мелкие категории, в зависимости от предназначения поврежденных бластных элементов.
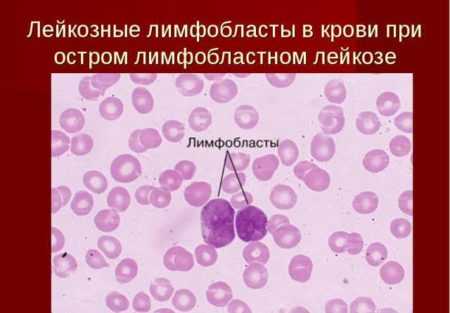 Острый лимфобластный лейкоз
Острый лимфобластный лейкозОбозначаться могут, например: острый В-лимфобластный лейкоз, что подразумевает сбой в создании бластов на уровне «производства» таких элементов, как В-лимфоциты или острый монобластный лейкоз, который возник при проблемах в создании моноцитов. В зависимости от степени сложности и вида лейкоза прогнозы на излечение пациента разные.
Какова норма бластных телец?
Бластные клетки в анализе крови не имеют нормы. В хорошем состоянии организма, когда отсутствуют стрессы и заболевания, стандартным количеством таких элементов в костном мозге будет 1 %. Они постепенно заменяют «отработавшие свое» элементы, и кроветворный орган восполняет эту недостачу, не превышая нормы.
В случае стресса, вирусной или бактериальной инфекции, костный мозг увеличит количество бластных телец до 10%. В исключительных случаях количество может быть немного больше. Любые другие показатели означают отклонения в работе системы.
Если число бластных телец доходит до 20% – это означает, что развивается такое заболевание, как острый лейкоз. Они бывают разных видов и форм, протекают быстро и относятся к раковым заболеваниям. Такое отклонение может проявиться совершенно неожиданно, даже у тех, кто в жизни не болел ничем серьезным. Это случается с детьми и людьми молодого возраста. У старшего поколения лейкозы вторичного характера, вызванные заболеваниями или лечениями, например: химиотерапией.
Что значат бластные клетки в анализе крови, норма которых превышена? На самом деле такие тельца в «незрелом» виде не должны выходить за пределы костного мозга. Туда отправляются полностью сформировавшиеся по предназначению элементы, которые готовы выполнять свою функцию. Если бласты в крови, это свидетельствует о запущенном раке.
Из вышесказанного можно сделать выводы:
- Бластные тельца должны отсутствовать в крови, их нормальное место обитание – костный мозг.
- В обычном состоянии такие элементы не должны превышать 1% от количества крови.
- До 10% бластных телец находится в костном мозге во время острой необходимости (болезни, инфекции).
- Более 20 % в костном мозге и нахождение деформиованных бласт в крови означают наличие острого лейкоза.
Точный диагноз, определяющий наличие лейкоза, можно поставить и до попадания бласт в кровь. Для этого достаточно общего клинического анализа крови, на котором виден уровень эритроцитов и другие сопутствующие показатели.
 Своевременная диагностика увеличивает шансы на успешное лечение
Своевременная диагностика увеличивает шансы на успешное лечениеЗаболеть острым лейкозом может человек, кошка, собака или другое живое существо, имеющее соответствующее строение тела. В любом случае это серьезное раковое заболевание, которое требует немедленного лечения. Шансы на успешный исход зависят от стадии заболевания, состояния и здоровья больного, вида лейкоза.
lechiserdce.ru
анализ на бласты, норма количества
 Бластами называют незрелые формы кровяных клеток. В целом они созревают до конца именно в костном мозге. А их появление в анализе крови в большинстве случаев свидетельствует о серьезных проблемах со здоровьем. Пациенту необходима срочная консультация врача-онколога. Определят это соответствующий анализ крови — бласты есть в жидкости или нет.
Бластами называют незрелые формы кровяных клеток. В целом они созревают до конца именно в костном мозге. А их появление в анализе крови в большинстве случаев свидетельствует о серьезных проблемах со здоровьем. Пациенту необходима срочная консультация врача-онколога. Определят это соответствующий анализ крови — бласты есть в жидкости или нет.
Эти клетки могут быть нормальными и злокачественными. Нормальные всегда имеются в костном мозге, правда, их там очень мало, количество не превышает 5 процентов.
А вот при лейкозах в разных формах их число настолько повышается, что они могут попадать не только во всевозможные органы и ткани (особенно в почки, головной мозг, селезенку, лимфатический узлы и печень), но также порой оказаться замеченными и в крови.
Иногда при постановке диагноза доктор указывает «лейкоз». Все потому, что обсуждаемые клетки очень схожи с лейкоцитами. Бласты в крови это молодые кровяные клетки, которые отличаются от других в составе жидкости строением своего ядра. Главным их признаком является содержание до пяти ядер в одной клетке.
В редких случаях появляются они в жидкости после аплазии. Ведь в этот период костный мозг изо всех сил восстанавливает свою работу. Но в основном это не злокачественные бласты, и появляются они в количестве не более двух процентов.
При любых других условиях не должны содержаться у здорового человека бласты в крови, норма их должна составлять ноль.
Причины
Как правило, причиной такого изменения анализа становится опасное заболевание — острый лейкоз. Если бластная клетка здорова, то со временем она вырастает в какую-либо полезную для организма клетку. И в кровь бласта при нормальных условиях никогда не попадет, оставаясь в костном мозге.
Только если пациенту вдруг необходимо много каких-то клеток при определенном заболевании, например, при тяжелой инфекции — лейкоцитов. В этом случае организм может начать активнее вырабатывать обсуждаемые клетки. Но все же их число все равно не может превысить 10 процентов, если у пациента нет никакого серьезного заболевания.
А вот бласты, которые начинают появляться в организме при остром лейкозе, совершенно иные. Они появляются как «трутни», питаются за счет запасов организма, но при этом не работают и не развиваются в полезные клетки, а наоборот создают себе подобных. Лейкозные бласты в итоге даже начинают «выгонять» здоровые нормальные клетки из их мест обитания и поселяются вместо них сами. Из-за этого появляются серьезные проблемы. Быстро идут на спад лейкоциты, гемоглобин и тромбоциты.
Пациент начинает ощущать неприятные симптомы в виде повышения температуры тела и появления слабости во всем теле.
 Если специалист выясняет, что количество бластов в крови сильно превышено, то, ему может быть поставлен соответствующий диагноз. При остром лейкозе в костном мозге их появляется более 20 процентов. Далее больному выполняют проточную цитометрию этих клеток, чтобы можно было точно определить, какой именно у него развивается лейкоз.
Если специалист выясняет, что количество бластов в крови сильно превышено, то, ему может быть поставлен соответствующий диагноз. При остром лейкозе в костном мозге их появляется более 20 процентов. Далее больному выполняют проточную цитометрию этих клеток, чтобы можно было точно определить, какой именно у него развивается лейкоз.
Что касается постановки диагноза и выбора терапии для пациента, то доверять в этом случае можно только грамотному опытному специалисту.
После того, как с помощью анализа он точно выяснит, что бласты в крови увеличились и причину этого изменения — далее сможет выбрать комплексное лечение, которое окажется подходящим для пациента — наиболее эффективным и безопасным. А вот самолечение в данном случае категорически противопоказано. Особенно рецепты народной медицины, которыми на сегодняшний день заполнен интернет. Такое лечение может значительно ухудшить самочувствие пациента и здоровье в целом.
oboleznjah.ru
что это такое, норма, расшифровка
Бласты – несозревшие клетки, из которых со временем формируются кровяные тельца. Бласты концентрируются в костном мозге, и в нем же проходит их превращение в компоненты, из которых состоит кровь.
Наличие бластов в анализе крови – очень тревожный знак. Это предтеча серьезных проблем со здоровьем. При разных формах лейкоза количество бластов неуклонно возрастает, они перенасыщают кровь и впоследствии проникают в каждую ткань и каждый орган. В мозг, печень, селезенку, почки и лимфатические узлы бласты попадают в первую очередь.
Особенность бластов в том, что в каждую их клетку может вмещаться до пяти ядер. В редчайших случаях бласты появляются в жидкости после аплазии, потому что как раз в это время приходит в норму функционирование костного мозга. Такие бласты практически не бывают злокачественными, и их концентрация в анализе не превышает нескольких процентов.
Читайте также: Как правильно сдавать биохимический анализ крови
Такие случаи – исключения. У здорового человека не может быть бластов в результате анализа крови. Их норма – это их отсутствие в крови.
Бластная клетка с нормальной фазой развития всегда будет находиться в костном мозге, и никогда не станет проникать в другие органы. Из нее со временем сформируется полезная клетка.
Если нарушается процесс создания новых клеток, то они уже не смогут снова стать полезными крови и организму. Они превращаются в паразитов, начинают пожирать полезные вещества вместо того, чтобы взаимодействовать с ними и переносить их. Дефектные клетки стремительно поглощают здоровые, тотчас сказываясь на результате анализа крови: в нем будет резкое падение лейкоцитов, гемоглобина и тромбоцитов.
Появление бластов в результатах анализа крови связывают с лейкозом. Зачастую попадание бластов в кровь сказывается на самочувствии человека:
- Ощущается постоянная слабость во всем теле.
- Температура тела часто повышена без видимой причины.
Эта аномалия поражает людей без поправки на возраст. Болезнь может развиться как у ребенка, так и у взрослых.
Лейкоз бывает:
- Хроническим – происходит поражение уже созревших клеток или лейкоцитов в стадии созревания.
- Острым – под удар попадают молодые клетки крови, преимущественно второго и третьего поколения. Бластов в крови при таком диагнозе может быть до шестидесяти процентов. Дополнительно в крови порой не оказываются клетки в промежуточной форме. Такое отсутствие получило название «лейкемический провал».
Если у человека по результатам анализа все указывает на лейкоз, то врач дополнительно назначает еще одно исследование – проточную цитометрию. Он определяет, на какой стадии развития находится лейкоз. И уже потом врач разрабатывает программу лечения, сугубо индивидуальную для каждого пациента. Категорически не рекомендуется самостоятельно назначать себе лекарства. Рецепты из «народной медицины» в лучшем случае не помогут, а в худшем – значительно усугубят здоровье и затруднят его последующее лечение.
Читайте также: Какими в норме должны быть активированные лимфоциты в анализе крови у ребенка
Бластные клетки в анализе крови: что это такое, норма, расшифровка
Нормы для количества бластов в крови не существует. Если человек здоров, у него нет ни намека на какое-либо заболевание, к тому же он не подвержен стрессу, то примерной нормой станет один процент содержания бластов в костном мозге. Бласты вытесняют из крови уже не несущие пользы клетки, заменяя их новыми.
Если человек долго находится в состоянии стресса или же его организм атакован бактериальными или вирусными инфекциями, то костный мозг начнет производить большее количество бластов. В процентном соотношении их количество возрастет до десяти процентов. В зависимости от того, что именно происходит с организмом, содержание может повысится максимум на несколько процентов больше. В случае если разница слишком велика, это является свидетельством зарождения серьезных отклонений в работе организма.
Когда количество бластов возрастает до двадцати процентов, то это означает стремительное развитие острого лейкоза. Только врач может определить, какой прогноз будет самым оптимальным при таком заболевании, и какого именно курса лечения следует придерживаться.
Незрелые бласты не должны попадать куда-то кроме костного мозга. За его пределы выходят уже сформированные элементы, которые уже пригодны к выполнению своих функций. Появление бластов в крови свидетельствует о том, что у человека раковое заболевание.
Чем раньше будет выявлена патология бластов, тем успешнее может быть процесс лечения. В запущенной форме и с общим негативным состоянием здоровья шансы вылечиться очень минимальны. Многое также зависит и от самого вида лейкоза, который поражает кровь.
Расшифровка анализа, обеспечение информации относительно того, какое обозначение имеет каждая позиция – прерогатива врача, а не пациента. Не имея специального образования, можно получить значительную дозу стресса, примеряя на себя фаталистические перспективы после получения результатов анализа.
obanalizekrovi.ru
Подсчет и анализ формулы костного мозга
Для оценки процессов кроветворения проводят составление и анализ миелограммы (формулы костного мозга), для чего необходимо предварительно получить красный костный мозг от пациента. Забор материала для анализа выполняют специальной иглой, которой пунктируют грудину в области рукоятки или подвздошной кости. Мазки красного костного мозга для изучения под микроскопом приготавливают так же, как и мазки крови для подсчета лейкоцитарной формулы.В ходе микроскопического исследования производят подсчет и исследование клеток красного костного мозга в предварительно окрашенных и зафиксированных мазках. Помимо микроскопа, для проведения анализа требуется специальная камера Горяева, в которой и происходит подсчет числа миелокариоцитов (имеющих ядра клеток-предшественников форменных элементов крови) в 5 или 100 больших квадратах.
При исследовании мазков красного костного мозга число миелокариоцитов определяют двумя способами.
Количество миелокариоцитов считается соответствующим норме, если при просмотре препарата красного костного мозга под микроскопом в каждом поле зрения наблюдается 15-25 клеток. При меньшем их количестве костный мозг оценивается как гипоклеточный, а если миелокариоцитов более 25, то как гиперклеточный.
Для подсчета мегакариоцитов (самых больших ядерных клеток красного костного мозга, образующих тромбоциты) также используют камеру Горяева. Число гигантских клеток рассчитывают по формуле.
В норме количество мегакариоцитов составляет (50,0 — 150,0) х 106 в 1 л.
При микроскопическом изучении мазка красного костного мозга наличие в поле зрения более 2-3 гигантских клеток считается нормальным.
Результат подсчета процентного соотношения форменных элементов красного костного мозга получил название миелограммы. После ее составления проводят морфологическую оценку отдельных элементов красного костного мозга. Следует помнить, что заключение ставят при непременном сопоставлении миелограммы с результатами гемограммы (общего анализа крови).
Нормальные показатели миелограммы представлены в таблице.
Нормальные показатели миелограммы
| Параметр | Показатель нормы | |||||
| У взрослых | У новорожденных | Возраст 3 года | Возраст 5-6 лет | |||
| Количество миелокариоцитов, X 109/л | 41,6- 195,0 | 146,5- 222,5 | 170,8- 296,8 | 100,4- 300,0 | ||
| Количество мегакариоцитов, X 106/л | 50,0- 150,0 | 51,8- 108,2 | 53,8- 113,8 | 52,8- 157,2 | ||
| Бластные клетки, % | 0,1-1,1 | 0,7-2,1 | 1,3-2,7 | 0-1,2 | ||
| Миелобласты, % | 0,2-1,7 | 0,8-1,8 | 0,8-3,3 | 1,5-3,6 | ||
| Не йт ро фи ль ные кл ет ки % | Не зр ел ые | Промиелоциты | 1,0-4,1 | 4,2-6,2 | 2,8-5,8 | 1,2-3,8 |
| Миелоциты | 7,0- 12,2 | 8,1- 12,3 | 8,5- 11,9 | 4,2-8,7 | ||
| Метамиелоциты | 8,0- 15,0 | 6,8-8,8 | 7,1-9,0 | 6,5- 10,3 | ||
| Зр ел ые | Палочкоядерные | 12,8- 23,7 | 20,0- 25,2 | 14,0- 25,4 | 13,2- 24,0 | |
| Сегментоядерные | 13,1- 24,1 | 18,0- 23,6 | 13,3- 22,5 | 8,3- 13,9 | ||
| Все нейтрофильные клетки, % | 52,7- 68,9 | 43,0- 54,7 | ||||
| Эозинофилы всех генераций, % | 0,5-5,8 | 2,7-5,3 | 2,8-6,8 | 2,4-7,4 | ||
| Базофилы, % | 0-0,5 | 0-0,3 | 0-0,1 | 0,2-0,8 | ||
| Лимфоциты, % | 4,3- 13,7 | 2,0-3,8 | 6,7- 14,6 | 18,7- 29,5 | ||
| Моноциты, % | 0,7-3,1 | 0-0,1 | 0-0,2 | 1,8-5,5 | ||
| Плазматические клетки, % | 0,1-1,8 | 0,1-0,1 | 0-0,3 | 0-0,5 | ||
| Эритробласты, % | 0,2-1,1 | 1,0-1,8 | 0,8-2,0 | 0,3-1,0 | ||
| Пронормобласты, % | 0,1-1,2 | |||||
| Нормо- бласты % | Базофильные | 1,4-4,6 | 2,5-5,1 | 1,4-3,4 | 1,2-2,4 | |
| Полихроматофильные | 8,9- 16,9 | 6,9- 10,6 | 7,5- 11,2 | 7,8- 16,0 | ||
| Оксифильные | 0,8-5,6 | 5,9- 10,0 | 5,5-7,3 | 0,1-1,9 | ||
| Все эритроидные клетки (эритрока- риоциты), % | 14,5- 26,5 | 11,3- 19,4 | ||||
| Ретикулярные клетки | 0,1-1,6 | 0,6-1,9 | 0,1-1,4 | 0,2-1,2 | ||
| Лейкоэритробластное отношение | 2,1-4,5 | |||||
| Индекс созревания эритрокариоцитов | 0,8-0,9 | |||||
| Индекс созревания нейтрофилов | 0,5-0,9 | |||||
В описании миелограммы врач обязан отметить морфологические признаки патологически измененных клеток (размер, форму клеток и ядер, соотношение объема ядра и цитоплазмы, характер хроматина, наличие нуклеол, цвет и зернистость цитоплазмы и т.п.), а также наличие качественных и количественных особенностей отдельных ростков органа кроветворения.
Анализ миелограммы осуществляется согласно определенной схеме, представленной в таблице 8.
Анализ миелограммы
| Параметр | Описание |
| Клеточность исследуемого материала(красного костного мозга) | нормальная |
| сниженная | |
| повышенная | |
| Состав пунктата по морфологическим характеристикам клеток (размер, форма клеток и ядер, соотношение ядра и цитоплазмы, характер хроматина, наличие нуклеол, цвет и зернистость цитоплазмы) | полиморфный (различный) |
| мономорфный (однообразный) | |
| значительно разведен периферической кровью | |
| Бласты | Количество и морфологическая характеристика |
| Гранулоцитарный росток | сохранен |
| сужен (редуцирован) | |
| расширен | |
| морфологическая характеристика клеток | |
| Созревание нейтрофилов | не нарушено |
| задержано | |
| ускорено | |
| Другие лейкоцитарные ростки | Количество и морфологическая характеристика клеток гиперплазирован- ного ростка |
| Эритроидный росток | сохранен |
| сужен (редуцирован) | |
| расширен | |
| морфологическая характеристика клеток | |
| Тип эритропоэза | нормобластный |
| мегалобластный | |
| Гемоглобинизация эритроцитов | не нарушена |
| ускорена | |
| задержана: на полихроматофиль- ных эритроцитах; на базофильных эри троцитах | |
| Параметр | Описание |
| Мегакариоциты | Количество и морфологическая характеристика клеток |
| Клетки злокачественного новообразования (эпителиальной природы) | обнаружены |
| не обнаружены |
Существуют индексы, позволяющие охарактеризовать кроветворение в красном костном мозге.
К их числу относят:
1) индекс созревания нейтрофилов;
2) лейкоэритробластное отношение;
3) индекс созревания эритрокариоцитов;
4) парциальная эритронормобластограмма.
Индекс созревания нейтрофилов (ИСН). Отражает соотношение незрелых и зрелых нейтрофилов костного мозга и рассчитывается по формуле:
ИСН = (ПроМц + Мц + МетаМц) : (П/Я + С/Я),
где ПроМц — промиелоциты;
Мц — миелоциты;
МетаМц — метамиелоциты;
П/Я — палочкоядерные нейтрофильные лейкоциты;
С/Я — сегментоядерные нейтрофильные лейкоциты.
В норме ИСН составляет 0,5-0,9. Повышение индекса созревания нейтрофилов при нормальной или повышенной клеточности пунктата расценивается как гиперплазия клеток белого ростка костного мозга (лейкопоэза). При пониженной клеточности пунктата может иметь место сужение эритроидного ростка красного костного мозга или значительная примесь периферической крови.
Снижение индекса созревания нейтрофилов при высокой клеточности пунктата является признаком разрастания клеток красного ряда; при пониженной клеточности пунктата — признаком угнетения процесса образования белых клеток, т. е. сужения белого ростка костного мозга (лейкопоэза).
Лейкоэритробластное соотношение (Л/Э). Определяет соотношение всех клеток (гранулоцитарных, моноцитарных и лимфоидных) белого ростка костного мозга к ядросодержащим клеткам эритроидного ряда.
В норме лейкоэритробластное соотношение равно 2,1-4,5.
Индекс созревания эритрокариоцитов (ИСЭ). Отражает соотношение гемоглобинизированных эритрокариоцитов и всех клеток эритроидного ряда: ИСЭ = (полихроматофильные нормобласты + оксифильные нормобласты): общее количество эритрокариоцитов.
Нормальные значения ИСЭ составляют 0,8-0,9.
Парциальная эритронормобластограмма. Определяет соотношение базофильных (эритробласты + базофильные нормобласты), полихроматофильных и оксифильных форм эритрокариоцитов.
Нормальное соотношение эритрокариоцитов : (базофильные клетки) : (полихроматофильные клетки) : (оксифильные клетки) = 1 : (2 :4) : (1,5 : 2).
analizy.vse-zabolevaniya.ru
005. МИЕЛОДИСПЛАСТИЧЕСКИЙ СИНДРОМ
Материалы представлены из учебного пособия РУДН
Анемии. Клиника, диагностика и лечение / Стуклов Н.И., Альпидовский В.К., Огурцов П.П. – М.: ООО «Медицинское информационное агентство», 2013. – 264 с.
Копирование и тиражирование материалов без указания авторов запрещено и преследуется по закону.
Миелодиспластический синдром (МДС) объединяет группу приобретенных заболеваний кроветворной системы, при которой патологический процесс начинается на уровне полипотентной стволовой клетки и обнаруживает себя нарушением пролиферации и дифференцировки клеток одного, двух или трех ростков кроветворения с их последующей гибелью в костном мозге (неэффективный эритропоэз).
В отличие от АА, стволовые клетки присутствуют в костном мозге больных МДС, хотя они функционально неполноценны. Костный мозг при МДС чаще бывает гиперклеточным, нормоклеточным и реже – гипоклеточным, тогда как в периферической крови обнаруживается рефрактерная анемия, нередко лейко- и/или тромбоцитопения.
В основе функциональной патологии полипотентных стволовых клеток лежат хромосомные изменения, которые обнаруживаются у большинства больных МДС. Они имеют клональный характер, аналогичный цитогенетическим изменениям при лейкозах. Хромосомные изменения при МДС разнообразны и включают транслокацию, инверсию и делецию хромосом. К наиболее характерным относятся: трисомия 8, моносомия 5, моносомия 7, делеция Y-хромосомы, делеция длинного плеча 7 (7q-), 11 (11q-), 13 (13q-), 20 (20q-), а также транслокации t(1;3), t(5;7), t(2;11), t(6;9), t(11;27), инверсия 3 хромосомы. У 20% больных наблюдаются множественные нарушения. Часто встречается делеция длинного плеча хромосомы 5 (у 30% больных). Причем установлено, что с этим плечом 5 хромосомы утрачиваются гены, отвечающие за синтез многих ростковых факторов, в том числе гранулоцитарно-макрофагального, ИЛ-3, ИЛ-4, ИЛ-5, ИЛ-6 и многих других биологически активных веществ, регулирующих кроветворение.
Форма с подобной хромосомной патологией была даже выделена среди больных МДС в 5q-синдром, который чаще встречается у женщин, характеризуется рефрактерной мегалобластной анемией и редко трансформируется в острый лейкоз (менее 5% больных).
Причины, вызывающие хромосомную патологию, неясны. В ряде случаев предполагается действие таких мутагенных факторов, как ионизирующая радиация, действие химических и лекарственных факторов.
Возникшая в костном мозге в одной полипотентной стволовой клетке цитогенетическая патология, обуславливающая в дальнейшем развитие МДС, способна воспроизводиться в потомках смутировавшей стволовой клетки, формируя таким образом патологический клон, клетки которого не способны к нормальной пролиферации и дифференцировке, что внешне проявляется их морфологической дисплазией и последующей костномозговой гибелью (неэффективный эритропоэз). Установлено, что 75% костного мозга при МДС имеют CD95, маркер запрограммированной клеточной гибели – апоптоза. Это обуславливает различные типы цитопений в периферической крови больных МДС.
Заболеваемость МДС составляет 3 – 15 случаев на 100000 населения и частота его повышается до 30 случаев у людей старше 70 лет и 70 случаев – в возрасте старше 80 лет. Средний возраст больных – 60 – 65 лет, у детей МДС встречается крайне редко.
Клиника
Клиническая картина МДС не имеет специфических особенностей. Основные симптомы зависят от глубины и сочетания поражения ростков кроветворения. Основным признаком болезни является рефрактерный анемический синдром, проявляющийся нарастающей слабостью, повышенной утомляемостью и другими свойственными анемии симптомами. У больных МДС с лейкопенией нередко возникают инфекционные осложнения (бронхиты, пневмонии идр.). Геморрагический синдром вследствие тромбоцитопении наблюдается у 10 – 30% больных, и проявляется кровоизлияниями на коже и видимых слизистых, кровоточивостью десен и носовыми кровотечениями.
Какой – либо характерной органной патологии при МДС нет: периферические лимфоузлы, печень и селезенка не увеличены.
Лабораторные данные.
Анемия различной степени выраженности наблюдается практически у всех больных МДС и чаще носит макроцитарный характер. Очень редко наблюдается гипохромия эритроцитов. Нередко присутствуют эллиптоциты, стоматоциты и акантоциты, а также базофильная пунктация и тельца Жолли в эритроцитах. В крови могут присутствовать ядросодержащие клетки красного ряда. Количество ретикулоцитов чаще сниженное.
Часто у больных в анализах крови имеется стойкая нейтропения, причем для гранулоцитов характерно наличие псевдопельгеровской аномалии (лейкоциты с двудольчатыми ядрами и дегрануляцией цитоплазмы).
Тромбоцитопения встречается у половины больных МДС. Среди тромбоцитов встречаются гигантские и дегранулированные формы.
У части больных МДС в анализах крови могут встречаться бластные клетки.
Костный мозг при МДС обычно гиперклеточный, но может быть нормоклеточным, а в редких случаях – даже гипоклеточным. Однако, всегда присутствуют черты дисэритропоэза: мегалобластоидность, многоядерность эритробластов, наличие митозов, патологических делений и ядерных аномалий, мостиков между ними, базофильная пунктация и вакуолизация цитоплазмы. У части больных в костном мозге повышено содержание сидеробластов с кольцевым расположением гранул железа вокруг ядра клетки.
Нарушение дифференцировки предшественников эритроцитов при МДС проявляется повышенным содержанием в них HbF (уровень которого в зрелых эритроцитах нормальный) и наличием в эритробластах пероксидазы и щелочной фосфатазы, что является характерным для нейтрофилов.
Дисгранулоцитопоэз в костном мозге проявляется задержкой созревания гранулоцитов на уровне миелоцитов, нарушением процесса грануляции цитоплазмы и снижением активности щелочной фосфатазы, что свидетельствует об их функциональной неполноценности, часто встречается гипо – или гиперсегментация ядер нейтрофилов.
Дисмегакариоцитопоэз характеризуется преобладанием микроформ и нарушенной отшнуровкой тромбоцитов.
При некоторых формах МДС выявляется повышенное содержание в костном мозге бластных клеток (от 5 до 20%).
При гистологическом исследовании костного мозга, полученного методом трепанобиопсии, у ряда больных имеет место повышенное образование ретикулиновых волокон, причем резко выраженный миелофиброз наблюдается у 10 – 15% больных МДС. Этому варианту МДС, характеризующемуся более выраженной гиперплазией и дисплазией клеток мегакариоцитарного ростка, с почти 100% наличием хромосомных аномалий, свойственны более выраженная анемия, тромбоцитопения и относительно короткая продолжительность жизни больных (медиана выживаемости 9 – 10 мес.).
Диагностика МДС основывается на наличии рефрактерной анемии, устойчивой к терапии витамином B12, фолиевой кислотой, железом и другими гематиками, которая нередко сочетается с нейтро- и тромбоцитопенией и наличием в пунктате костного мозга морфологических признаков дисгематопоэза (нарушения созревания кроветворных клеток).
Классификация МДС:
В настоящее время в клинической практике используются две классификации: Франко-американо-британской группы (FAB) 1982 года и Всемирной организации здравоохранения (ВОЗ) 2008 годам.
Дифференциальный диагноз
РА чаще всего приходится дифференцировать от витамин-B12— и фолиево-дефицитной анемий, при которых также имеется мегалобластное кроветворение и морфологические признаки дисплазии клеток красного ростка, свидетельствующие о неэффективном эритропоэзе. Быстрые клинический и гематологический ответы на терапию витамином B12 или фолиевой кислотой указывают на причинную взаимосвязь между анемией и дефицитом этих витаминов.
РАКС необходимо дифференцировать с приобретенной сидеробластной анемией, обусловленной хронической свинцовой интоксикацией. РЦМД, при которой имеется панцитопения в периферической крови, напоминает апластическую анемию. Наличие нормальной клеточности костного мозга с морфологическими признаками дисмиелопоэза позволяет правильно верифицировать диагноз.
Классификация МДС (ВОЗ, 2008)
|
Нозологическая форма МДС |
Изменения в крови |
Изменения в костном мозге |
|
Рефрактерная анемия (РА) |
— анемия — бласты < 1% — моноциты < 1 х 109/л |
— дисплазия кроветворения < 10% в одном ростке кроветворения — бласты < 5% — кольцевые сидеробласты < 15% |
|
Рефрактерная нейтропения (РН) |
— нейтропения — бласты < 1% — моноциты < 1 х 109/л |
|
|
Рефрактерная тромбоцитопения (РТ) |
— тромбоцитопения — бласты < 1% — моноциты < 1 х 109/л |
|
|
Рефрактерная анемия с кольцевыми сидеробластами (РАКС) |
— анемия — бласты < 1% — моноциты < 1 х 109/л |
— дисплазия кроветворения. — бласты < 5% — кольцевые сидеробласты > 15% |
|
Рефрактерная цитопения с многоростковой дисплазией (РЦМД) |
— цитопения по 2 – 3 росткам — бласты < 1% — моноциты < 1 х 109/л |
— дисплазия кроветворения < 10% в двух и более ростках кроветворения — бласты < 5% — кольцевые сидеробласты (любое количество) |
|
Рефрактерная анемия с избытком бластов I (РАИБ-1) |
— цитопения любая — бласты < 5% — моноциты < 1 х 109/л |
— множественная дисплазия во всех ростках кроветворения — бласты 5 – 9% |
|
Рефрактерная анемия с избытком бластов II (РАИБ-2) |
— цитопения любая — бласты 5 – 19% — моноциты < 1 х 109/л |
— множественная дисплазия во всех ростках кроветворения — бласты 10 – 19% — палочки Ауэра ± |
|
МДС неклассифици-рованный (МДС-Н) |
— цитопения любая — бласты <1%
|
— дисплазия кроветворения < 10% в одном или несколь- ких ростках кроветворения — бласты < 5% |
|
Синдром 5q- |
— анемия — бласты < 1% — тромбоциты норма или увеличены
|
— нормальное или увеличенное количество мегакариоцитов с гипосегментированными ядрами — изолированная делеция 5q — бласты < 5% |
Гипопластический вариант МДС отличить от АА значительно труднее. В пользу гипоплазии при МДС говорит наличие хромосомной патологии, отсутствующей при АА, высокое содержание на гемопоэтических клетках проапоптических белков (CD95) и низкий уровень щелочной фосфатазы в гранулоцитах при МДС в отличие от нормального содержания этого фермента при АА.МДС с избытком бластов отличается от острого лейкоза по количественному содержанию бластных клеток в костном мозге: все случаи с бластозом более 20% рассматриваются как острый лейкоз.
Лечение
Симптоматическая терапия
Ведущее место в лечении МДС занимает поддерживающая терапия, в первую очередь – переливание эритроцитарной массы, сопровождающееся введением десферала или деферазирокса для удаления избытка железа. Переливание эритроцитарной массы показано при снижении уровня Hb до 80 г/л и ниже, а частота ее зависит от динамики показателей красной крови. Для борьбы с геморрагическим диатезом используется введение тромбоконцентрата, показания те же, что и при лечении АА. При инфекционных осложнениях, обусловленных гранулоцитопенией, показано введение антибиотиков.
Патогенетическая терапия зависит от количества бластов к костном мозге. При выраженом бластозе (> 10%) необходимо регулярно проводить стернальные пункции, чтобы исключить трансформацию МДС в острый лейкоз (acuteleukemia, AL). При увеличении бластов больше 20% терапия проводится по программам лечения AL.
Алгоритм лечения МДС (Савченко В.Г., Кохно А.В., Паровичникова Е.Н.)
|
Клеточность костного мозга |
|||
|
Гипоклеточный костный мозг |
Нормо/гиперклеточный костный мозг |
||
|
<5% бластов |
5 – 20% бластов |
<5% бластов |
5 – 20% бластов |
|
СуА |
СуА |
рчЭПО |
Децитабин, азацитидин |
|
АТГ |
АТГ |
Спленэктомия |
FLAG, 7 + 3 |
|
Спленэктомия |
Децитабин, азацитидин |
Интерферон-α |
МДЦ – 14 дней |
|
рчЭПО |
МДЦ – 14 дней, 6 – МП, мельфалан |
Децитабин, азацитидин |
6 – МП |
В случаях количества бластов в костном мозге стойко ниже 20% для принятия решения о тактике лечения необходимо проведение трепанобиопсии, которая позволяет установить клеточность костного мозга. После чего терапия МДС может быть направлена на стимулирование кроветворения при гипоплазии костного мозга (рекомбинантный человеческий эритропоэтин – рч-ЭПО), иммуносупрессию с целью активации стволовых клеток (АТГ, CyA), снижение гемолиза и секвестрации клеток крови (спленэктомия). При гиперклеточных вариантах или формах МДС с бластозом более 5% лечение должно включать подавление опухолевого роста (химиотерапию). В России наиболее подходящий алгоритм выбора терапии МДС, схема которого указана в таблице, сформулирован специалистами Гематологического научного центра: Савченко В.Г., Кохно А.В., Паровичниковой Е.Н. в 2012 году.
В последние годы для стимуляции эритропоэза у больных МДС, иногда успешно, используется рчЭПО: рекормон, эритростим, эпрекс, аранесп и др., который особенно эффективен при низкой концентрации в крови нативного ЭПО (< 500 ед/мл). РчЭПО рекомендуется применять в дозе 100000 МЕ 3 раза в неделю подкожно или по 30000 – 40000 МЕ раз в неделю (при использовании пролонгированных форм эритропоэтина). Терапия считается эффективной при приросте гемоглобина более чем на 10 г/л за 4 – 8 недель или снижение зависимости от гемотрансфузий. Целевая концентрация гемоглобина 120 г/л. Через 2 месяца лечения рчЭПО сообщается о положительном эффекте у 41,6% больных с РА и у 76% больных с РАКС, причем к 6 месяцу этот эффект сохраняется соответственно у 33% и 58%. Таким образом, наиболее эффективным применение ЭПО оказалось у больных при варианте МДС-РАКС.
У белее чем трети больных МДС тяжесть тромбоцитопении может быть временно снижена введением интерферона-α, это позволяет избежать аллоиммунизации, обусловленной введением тромбоконцентрата.Терапия глюкокортикоидами при МДС не эффективна, хотя иногда может уменьшить интенсивность геморрагического синдрома.
У больных МДС с гипопластической фазой заболевания, как и при АА, эффективным оказалось проведение иммуносупрессивной терапии (СуА), которая не только блокирует действие Т-клеток-супрессоров, но и ингибирует клеточный апоптоз. Циклоспорин А назначается в дозе 5 мг/кг и вызывает гематологическое улучшение у 60больных этой группы (полные ремиссии развиваются реже, частичное улучшение – чаще).
Для лечения форм МДС РА, РАКС, РЦМД в качестве первичного метода лечения у пожилых (старше 60 лет) больных с гипоплазией кроветворения или при резистентности к циклоспорину в настоящее время широко применяется спленэктомия с биопсией печении. Наряду с лечебным эффектом данный подход позволяет исключить другие причины развития дисплазии кроветворения. Как правил, спленэктомия позволяет добиться длительных перерывов в гемотрансфузиях, улучшить качество жизни больных.
Использование цитостатических препаратов при РАИБ-варианте МДС в настоящее время считается самым эффективным лечением. До недавнего времени в качестве патогенетической терапии применяли в основном малые дозы цитозара и мелфалан. Схема лечения малыми дозами цитозара выглядит следующим образом. Вводят подкожно по 10 мг/м2 2 раза в день в течение 14, 21 или 28 дней в зависимости от количества бластов и клеточности костного мозга. Мельфалан применяют в дозах 5 – 10 мг/м2 в течение 5 дней peros. Такие курсы проводят раз в месяц, как правило, отполугода до 3 лет, с оценкой терапевтического эффекта каждые 2 – 4 месяца. Эффективной терапия считается при нормализации или относительной нормализации показателей периферической крови и костного мозга, при отсутствии или резком снижении зависимости от гемотрансфузий. Использование указанных схем лечения приводит к развитию частичной ремиссии у 56% больных. Однако, на выживаемость больных такая терапия существенно не влияет.
При тяжелом состоянии больных и невозможности проведения адекватной терапии при МДС-РАИБ-1 и -2 возможно назначать 6-меркаптопурин по 60 мг/м2 в сутки peros в течение 3 лет.
В настоящее время делаются попытки использовать в лечении МДС талидомида и его аналога леналидомида, лишенного нейтротоксической активности, но являющегося мощным ингибитором протеаз. Применение леналидомида вызвало снижение трансфузионной зависимости у 67% больных, причем у 58% достигалась полная независимость от трансфузионной терапии. Стоит отметить, что этот препарат особенно эффективен при 5q-варианте МДС, где его эффективность равна 91%, тогда как при других нарушениях кариотипа – только 19%.
У молодых больных до 60 лет в стандарты лечения МДС-РАИБ-2 входит полихимиотерапия. Используют курсы, применяемые в лечении острых миелобластных лейкозах: «7 + 3» и «FLAG». «7 + 3»: цитарабин 100 мг/м2 в/в капельно каждые 12 часов 1 – 7 дни курса и идарубицин 12 мг/м2 в/в капельно 1 – 3 дни курса. «FLAG»: флударабин 25 мг/м2 в/в капельно 1 – 5 дни курса, цитарабин 2 г/м2 в/в капельно 1 – 5 дни курса + Г-КСФ (гранулоцитарный колониестимулирующий фактор) 5 мкг/кг п/к ежедневно до выхода из цитопении.
Из других активно разрабатываемых препаратов в гематологической практике заслуживают внимание триоксид мышьяка, бевацизумаб (авастин) и др.
В последнее время в клиническую практику внедрены современные цитостатические препараты ингибиторы ДНК-метилтрансфераз. Механизм их действия связан с ингибированием процесса метилирования ДНК в клетках опухолевого клона, что приводит к повышению активности генов, регулирующих клеточный цикл и нормализации процессов дифференцировки клеток костного мозга. Два основных вещества зарегестрированы в России под названием децитабин (Дакоген), азацитидин (Ведаза). По опубликованным данным крупнейших международных исследований эффективность использования этих препаратов в лечении МДС составила 50 – 70%. Децитабин вводят в дозе 20 мг/м2 в/в капельно 1 – 5 дни раз в месяц. Таких курсов проводят4, далее оценивают эффект. При положительной оценке продолжают терапию в течение долгого времени до развития осложнений, при отсутствии эффекта используют другие препараты. Азацитидин вводят подкожно 75 мг/м2 1 – 7 дни раз в месяц. Оценивают эффект через полгода, далее или продолжают терапию длительно или меняют препараты.
Необходимо знать, что самым серьезным осложнением химиотерапии, требующим иногда отмены лечения, является цитопения. Цитопения, как правило, проявляется снижением всех показателей крови (Hb, лейкоциты и тромбоциты). Тяжелыми состояниями, угрожающими жизни считается анемия менее 70 г/л, тромбоцитопения менее 20 х 109/л, лейкопения менее 1 х 109/л или нейтропения менее 0,5 х 109/л. Такие состояния требуют обязательного стационарного лечения, проведения трансфузионной и антибактериальной терапии.
Единственным радикальным методом лечения МДС могла бы стать аллогенная трансплантация костного мозга, однако, применение этого метода ограничивается пожилым возрастом больных, подавляющее большинство которых старше 60 лет.
Прогноз при МДС остается неблагоприятным и зависит от варианта МДС. При РА трансформация в острый лейкоз наблюдается у 15% больных, а медиана выживаемости составляет 50 месяцев. При РАКС эти показатели составляют соответственно 8% и 51 месяц; при РАИБ – 44% и 11 месяцев.
stuklov.ru
